Fertigarzneimittel
- Velcade®
- In einigen EU-Ländern sind mittlerweile Generika zugelassen
Indikation
Bortezomib ist ein Krebsmedikament zur Behandlung des multiplen Myeloms, einer Art von Blutkrebs, bei folgenden Patientengruppen:
- Erwachsene, deren Erkrankung sich nach Erhalt mindestens einer anderen Behandlung verschlimmert und die sich bereits einer Blutstammzelltransplantation unterzogen haben oder für eine Blutstammzelltransplantation nicht geeignet sind. Bortezomib wird bei diesen Patienten entweder als Monotherapie oder in Kombination mit pegyliertem liposomalem Doxorubicin oder Dexamethason angewendet;
- zuvor unbehandelte Erwachsene, die für eine Hochdosis-Chemotherapie zusammen mit einer Blutstammzelltransplantation nicht geeignet sind. Bei diesen Patienten wird Bortezomib in Kombination mit Melphalan und Prednison angewendet;
- zuvor unbehandelte Erwachsene, bei denen eine Behandlung mit einer Hochdosis-Chemotherapie gefolgt von einer Blutstammzelltransplantation ansteht. Bei dieser Patientengruppe wird Bortezomib in Kombination mit Dexamethason bzw. mit Dexamethason plus Thalidomid angewendet.
Bortezomib wird außerdem zur Behandlung des Mantelzell-Lymphoms, einer anderen Art von Blutkrebs, bei unbehandelten Erwachsenen angewendet, die für eine Blutstammzelltransplantation nicht geeignet sind. Beim Mantelzell-Lymphom wird Bortezomib in Kombination mit Rituximab, Cyclophosphamid, Doxorubicin und Prednison angewendet.
Anwendung
Bortezomib ist nur auf ärztliche Verschreibung erhältlich und die Behandlung sollte nur unter der Aufsicht eines Arztes eingeleitet und verabreicht werden, der Erfahrung in der Anwendung der Chemotherapie gegen Krebs hat.
Bortezomib ist in Durchstechflaschen als 3,5 mg-Pulver zur Herstellung einer Injektionslösung zur Injektion in eine Vene oder unter die Haut erhältlich. Bortezomib darf nicht auf andere Weise angewendet werden.
Die empfohlene Anfangsdosis beträgt 1,3 mg pro Quadratmeter Körperoberfläche (berechnet nach Größe und Gewicht des Patienten). Bei der Injektion in eine Vene wird die Lösung über 3 bis 5 Sekunden über einen Katheter (einen dünnen, sterilen Schlauch) injiziert. Zwischen zwei aufeinanderfolgenden Dosen Bortezomib müssen mindestens 72 Stunden liegen. Bei Injektion unter die Haut wird es in den Oberschenkel oder das Abdomen (Bauch) verabreicht.
Dosen von Bortezomib werden mit Unterbrechungen, d. h. mit Ruhepausen zwischen den Dosierungen, in Behandlungszyklen von drei bis sechs Wochen gegeben, je nachdem, ob Bortezomib allein oder in Kombination mit anderen Arzneimitteln angewendet wird. Treten bei dem Patienten nach einem Behandlungszyklus schwere Nebenwirkungen auf, muss die Behandlung abgesetzt oder verschoben oder die Dosis angepasst werden.
Dosisanpassung
Bei Patienten mit mittelschweren bis schweren Leberproblemen sollten niedrigere Dosen verwendet werden. Nähere Informationen zur Anwendung von Bortezomib sind der Zusammenfassung der Merkmale des Arzneimittels (ebenfalls Teil des EPAR) zu entnehmen.
Wirkmechanismus
Der Wirkstoff Bortezomib ist ein Proteasom-Inhibitor. Er blockiert das Proteasomensystem, ein System in den Zellen, das bestimmte Proteine reguliert und für das Überleben der Zelle notwendig ist. Die Blockierung des Proteasomensystems führt zum Absterben der Zelle. Krebszellen sind anfälliger als normale Zellen für eine Störung durch Proteasom-Hemmer und somit auch anfälliger für die Wirkung von Bortezomib.
Wirkstoffklasse: Proteasom-Inhibitor
Studienlage
In den Studien zu multiplem Myelom erwiesen sich sowohl die Monotherapie mit Bortezomib als auch die Kombinationstherapien mit Bortezomib für verschiedene Patientengruppen als vorteilhaft; die Hauptnutzen sind nachfolgend aufgelistet:
- Bei nicht vorbehandelten Patienten dauerte es durchschnittlich 20,7 Monate, bis sich ihre Erkrankung verschlimmerte, wenn sie Bortezomib zusammen mit Melphalan und Prednison erhielten, im Vergleich zu 15,0 Monaten bei denen, die nur Melphalan und Prednison erhielten.
- Bei vorbehandelten Patienten, die Velcade erhielten, dauerte es durchschnittlich 6,2 Monate, bei denen, die Dexamethason erhielten, durchschnittlich 3,5 Monate, bis sich ihre Erkrankung verschlimmerte.
- Etwa 34 % der Patienten sprachen teilweise oder vollständig auf die Behandlung mit Velcade an (in einer Studie, in der Velcade nicht mit einem anderen Arzneimittel verglichen wurde).
- In der Studie, in der der Injektionsort von Velcade – subkutan oder intravenös – verglichen wurde, war der prozentuale Anteil von Patienten, die teilweise oder vollständig auf die Behandlung ansprachen, bei beiden Anwendungsarten gleich (42 %).
- Etwa 15 % der Patienten, die für eine hoch dosierte Chemotherapie und eine Blutstammzellentransplantation vorgesehen waren, sprachen auf die Behandlung mit Velcade plus Dexamethason an, im Vergleich zu 6 % der Patienten, bei denen die Standardkombinationen angewendet wurden. Außerdem sprachen 49 % dieser Patienten auf die Kombinationstherapie aus Velcade plus Thalidomid und Dexamethason an, während nur etwa 26 % auf eine Behandlung mit Velcade plus anderen Antikrebsarzneimitteln und 17 % auf eine Behandlung mit Thalidomid und Dexamethason ansprachen.
- Bei Patienten, deren Erkrankung sich nach fehlendem Ansprechen auf mindestens eine andere Behandlung verschlimmert hatte, betrug die Dauer bis zu einer Verschlimmerung ihrer Erkrankung nach Anwendung von Velcade zusammen mit pegyliertem liposomalem Doxorubicin 9,3 Monate, verglichen mit 6,5 Monaten bei alleiniger Anwendung von Bortezomib.
- Von den Patienten, bei denen sich die Erkrankung verschlimmert hatte bzw. erneut aufgetreten war oder die auf mindestens eine andere Behandlung nicht angesprochen hatten, sprachen etwa 70% auf die Velcade/Dexamethason-Kombinationstherapie an.
Bei Mantelzelllymphom lebten Patienten, die mit einer Kombination aus Bortezomib plus Rituximab, Cyclophosphamid, Doxorubicin und Prednison behandelt wurden, länger ohne Verschlimmerung der Erkrankung (24,7 Monate) als Patienten, denen die gleiche Kombination, aber mit Vincristin statt Bortezomib gegeben wurde (14,4 Monate).
Unerwünschte Arzneimittelwirkungen – Nebenwirkungen
Sehr häufig berichtete Nebenwirkungen bei der Behandlung mit Bortezomib sind Nausea (Übelkeit), Diarrhö (Durchfall), Verstopfung, Erbrechen, Fatigue (Erschöpfung), Pyrexie (Fieber), Thrombozytopenie (verminderte Zahl der Blutplättchen), Anämie (verminderte Zahl der roten Blutkörperchen), Neutropenie (verminderte Zahl der Neutrophilen, einer Art weißer Blutkörperchen, die Infekte bekämpfen), periphere Neuropathie (Nervenschaden in Händen und Füßen), Kopfschmerzen, Parästhesie (ungewöhnliche Empfindungen wie Kribbeln und Prickeln), verminderter Appetit, Dyspnoe (Atembeschwerden), Hautausschlag, Herpes Zoster (Gürtelrose) und Myalgie (Muskelschmerzen).
Zu den schwerwiegendsten Nebenwirkungen zählen Herzinsuffizienz, Tumor-Lyse-Syndrom (Komplikationen durch den Abbau von Krebszellen), pulmonale Hypertonie (hoher Blutdruck in den Lungenarterien), posteriores reversibles Enzephalopatie-Syndrom (eine reversible Störung der Gehirnfunktion), akute diffuse infiltrative Lungeninfektion (eine schwere Lungenerkrankung) und autonome Neuropathie (Schädigung der Nerven, die Organe wie Blase, Augen, Darm, Herz und die Blutgefäße steuern). Die vollständige Auflistung der im Zusammenhang mit Velcade® berichteten Nebenwirkungen ist der Packungsbeilage zu entnehmen.
Kontraindikationen
Velcade® darf nicht bei Patienten angewendet werden, die überempfindlich (allergisch) gegen Bortezomib, Bor oder einen der sonstigen Bestandteile sind. Es darf nicht bei Patienten mit akuter diffuser infiltrativer Lungeninfektion oder perikardialer Erkrankung (einer Herzbeutelerkrankung) angewendet werden. Wird Velcade zusammen mit anderen Arzneimitteln angewendet, müssen auch die für diese Arzneimittel geltenden Einschränkungen, einschließlich der Anforderungen bezüglich Schwangerschaftstests und -verhütung in Verbindung mit Thalidomid, berücksichtigt werden.
Chemie
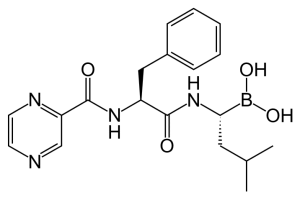
- ATC Code L01XX32
- DrugBank APRD00828
Literatur & Quellen
- Zusammenfassung des EPAR für die Öffentlichkeit; Velcade – Bortezomib;EMA/27714/2015 EMEA/H/C/000539; 01-2015 LINK